Грибок Candida связали с риском Альцгеймера
Вы только вдумайтесь: обычный грибок, который живет у каждого из нас во рту или на коже, вдруг оказался причастен к развитию болезни Альцгеймера. Звучит как сценарий фильма ужасов, но это данные нового исследования. Ученые наконец-то начинают распутывать этот детектив: как именно Candida albicans умудряется пробраться в мозг и запустить механизмы, ведущие к нейродегенерации.
Этот парень, Candida albicans, обычно ведет себя тихо и мирно, входя в компанию добропорядочных микробов на наших слизистых. Но стоит иммунитету дать слабину, как тихоня превращается в агрессора и может вызвать серьезные инфекции. И вот что странно: грибок находили в мозгах людей с Альцгеймером, но без типичных признаков воспаления — ни температуры, ни резкого ухудшения. Получается, инфекция может тлеть годами, оставаясь незамеченной, но делая свое черное дело.
Идея о том, что в основе болезни Альцгеймера может лежать инфекция, витает в воздухе уже давно. Еще в 2019 году та же группа ученых показала: Candida, попав в мозг, способна вызывать изменения, подозрительно похожие на альцгеймеровские.
Новое исследование в журнале Cell Reports пошло дальше и копнуло вглубь — на уровень молекулярных механизмов. Зачем грибку вообще сдался наш мозг и как ему удается там хозяйничать? «Это открытие может стать важным кусочком пазла», — говорит один из авторов, Дэвид Корри. И с ним трудно спорить.
Тихая война в черепной коробке: как грибок дурит наш иммунитет
Обычно, когда в организм вторгаются чужаки, иммунитет бьет в набат, созывая тяжелую артиллерию — макрофаги и нейтрофилы. Но тут всё пошло не по плану. Оказалось, что во время вялотекущей мозговой инфекции, вызванной Candida, эти солдаты почему-то не приходят. Вместо них активируется местная полиция — клетки микроглии. У здоровых мышей иммунитет справляется с грибком дней за десять, но как именно — долго оставалось загадкой. И главный вопрос: как грибок вообще умудряется пересечь неприступный гематоэнцефалический барьер?
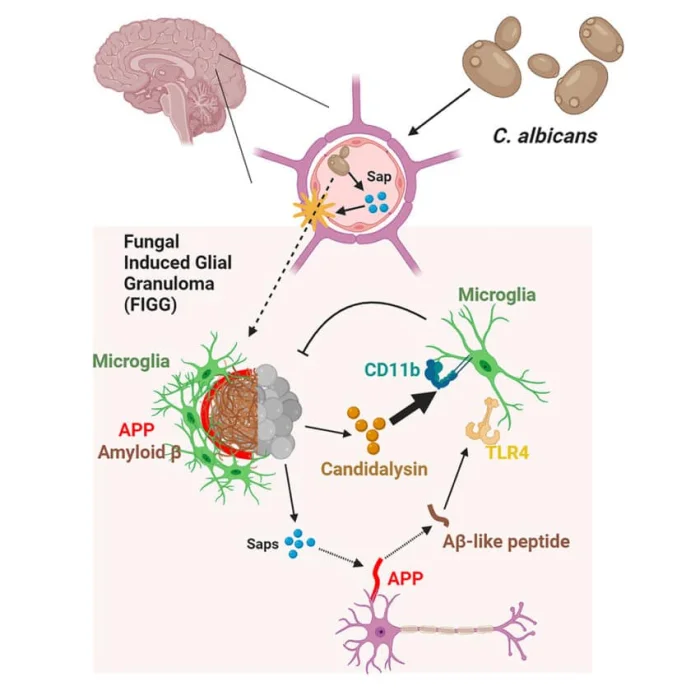
Ученые предположили, что Candida использует грубую силу. Грибок выделяет особые ферменты — протеиназы (Saps), способные разрезать практически любой человеческий белок. А наш гематоэнцефалический барьер держится как раз на плотных белковых «замках» между клетками. Логично: если разрезать замок, дверь откроется. Эксперименты на мышах подтвердили: так оно и есть.
Но самое интересное началось, когда грибок уже пробрался внутрь. Оказалось, что эти же ферменты, разрушая белки, нарезают и белок-предшественник амилоида (APP), который есть в наших нейронах. В результате образуются те самые пептиды, из которых потом собираются злополучные амилоидные бляшки. Иммунная система, видя эти обломки, пытается активироваться, чтобы уничтожить грибок. Это помогает сдерживать инфекцию, но полностью не убивает её.
Есть и второй механизм защиты. Грибок производит токсин кандидализин, который тоже будит микроглию, но через другой рецептор. Если этот путь заблокировать, инфекция становится хронической. «Активация микроглии через кандидализин критически важна для очистки мозга от Candida. Уберите этот механизм — и грибок останется с вами надолго«, — объясняет ведущий автор Ифань Ву.
И вот тут возникает главный парадокс: пытаясь защитить нас от грибка, иммунитет сам себе создает проблемы. Нарушение этих механизмов очистки приводит к тому, что токсичные амилоидные пептиды накапливаются. Раньше считалось, что эти пептиды — исключительно «внутренний брак» нашего собственного мозга. Теперь выясняется, что они могут быть и «продукцией», навязанной извне. «Скорее всего, амилоидные бляшки при нейродегенеративных заболеваниях, связанных с Candida, имеют двойное происхождение — и мозговое, и грибковое«, — добавляет Корри.
Знаете, что в этой истории самое обнадеживающее? Если бляшки могут возникать из-за грибка, значит, воздействуя на грибок, мы потенциально можем повлиять на развитие болезни. И это открывает совершенно новые горизонты для терапии, о которых раньше мы даже не задумывались.